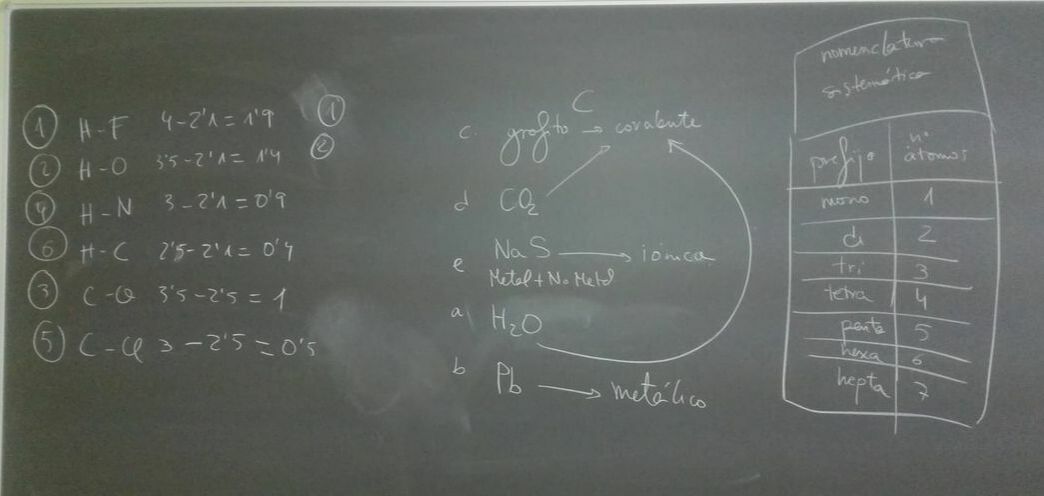
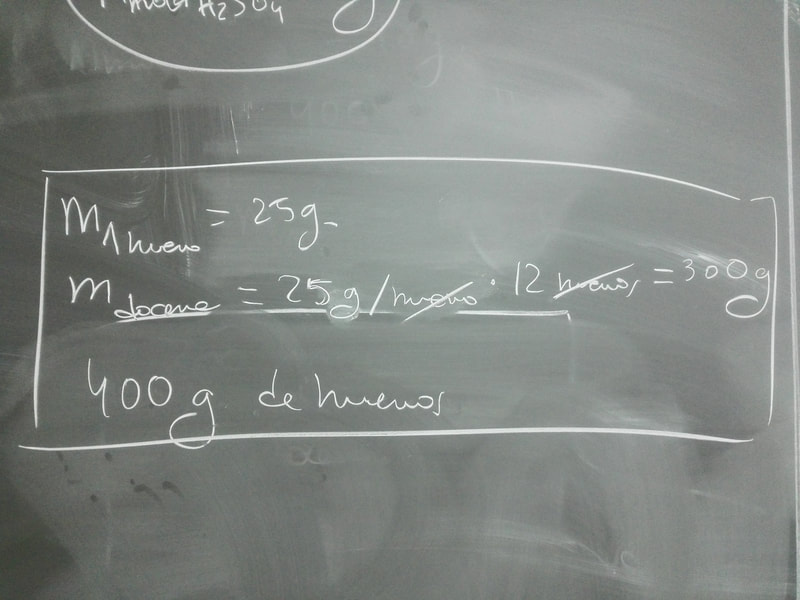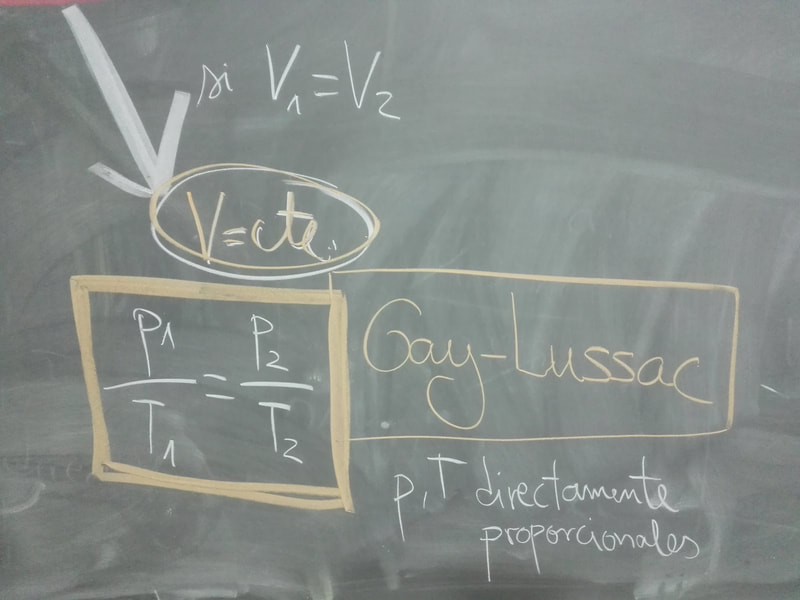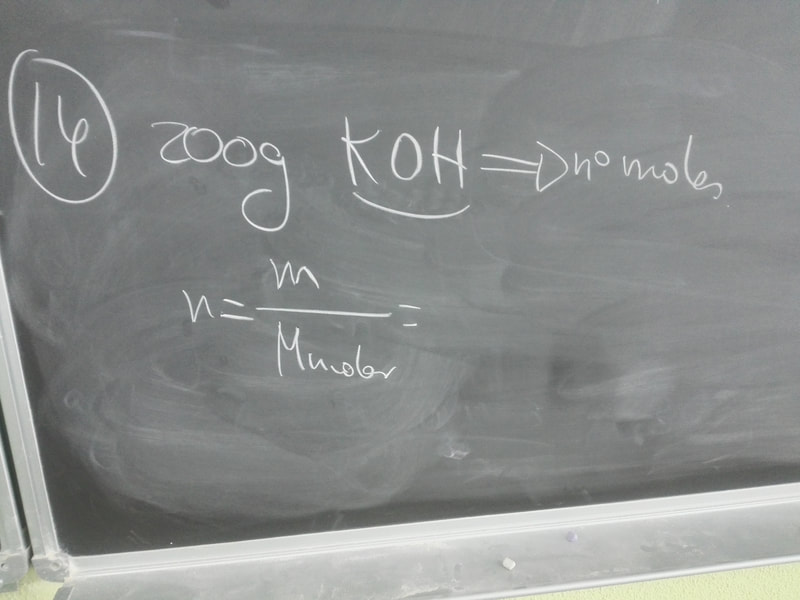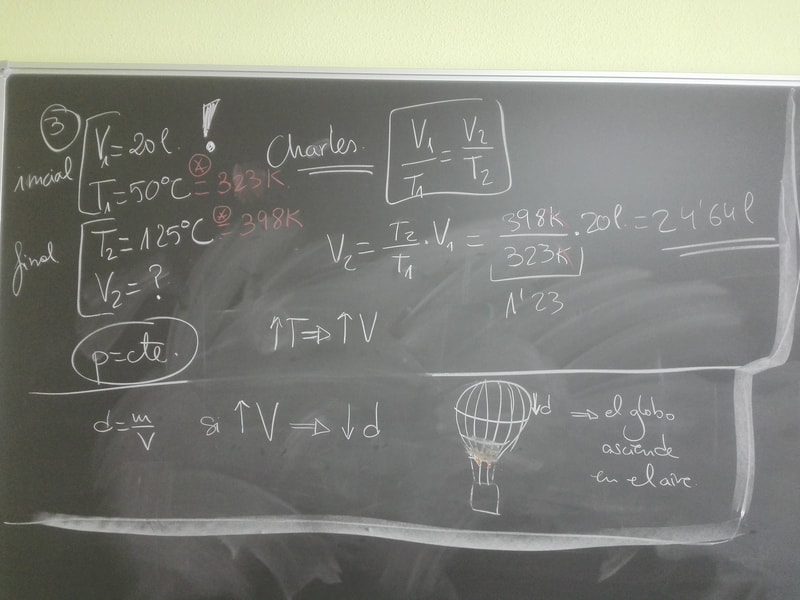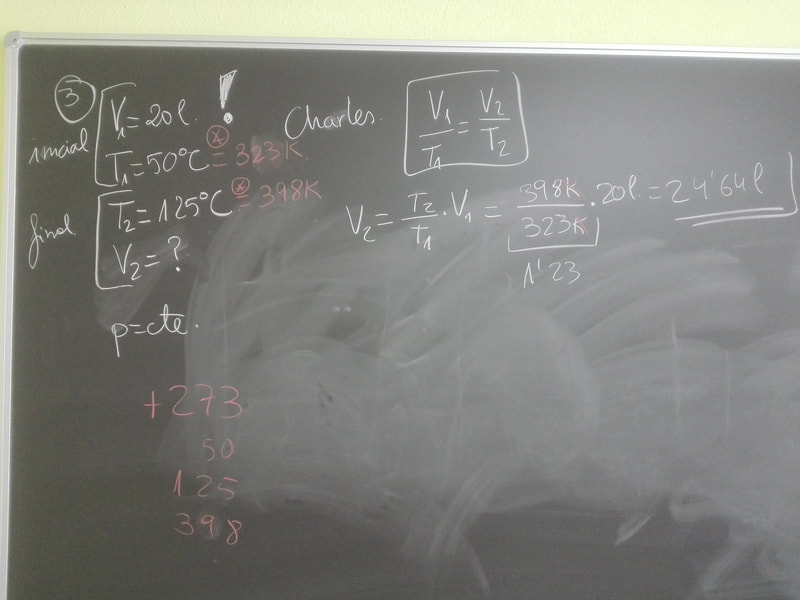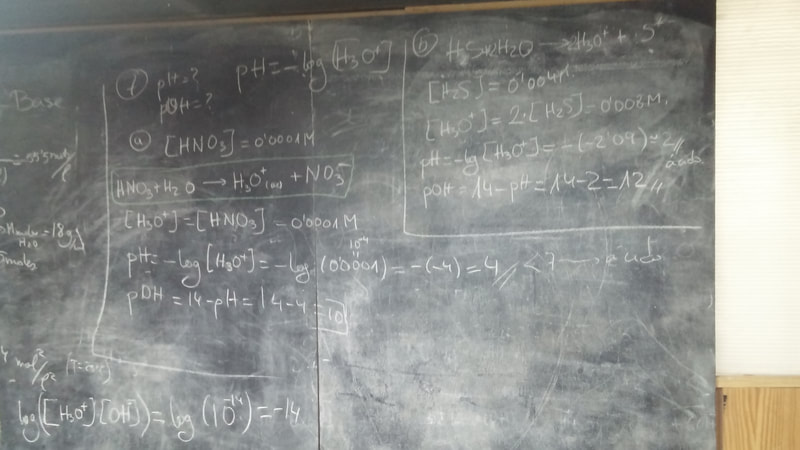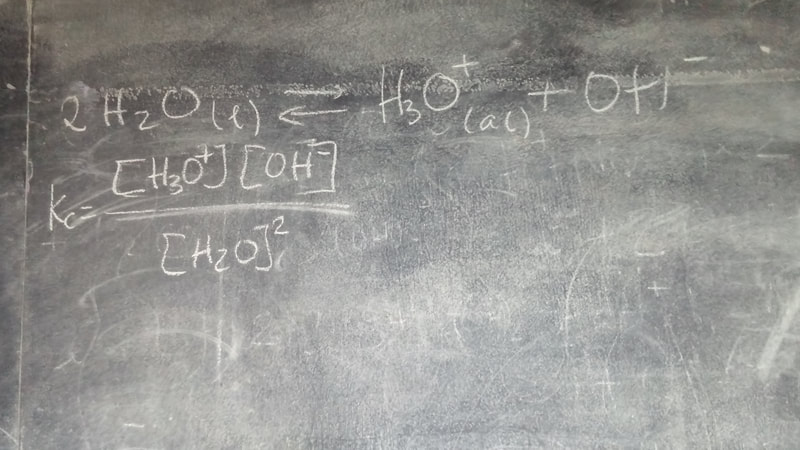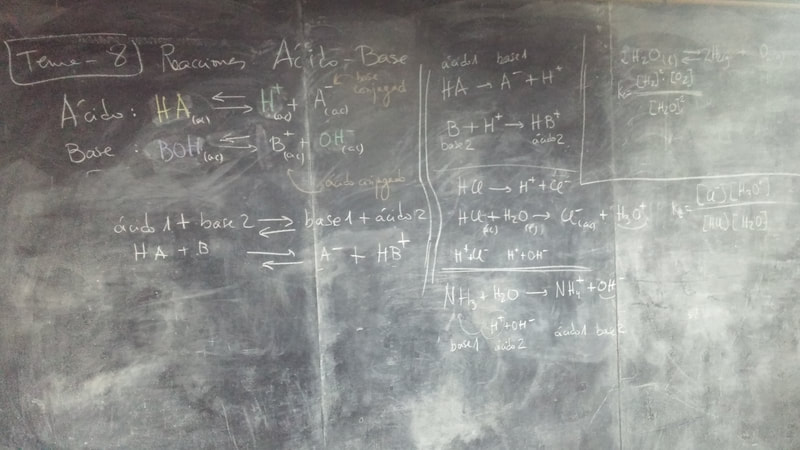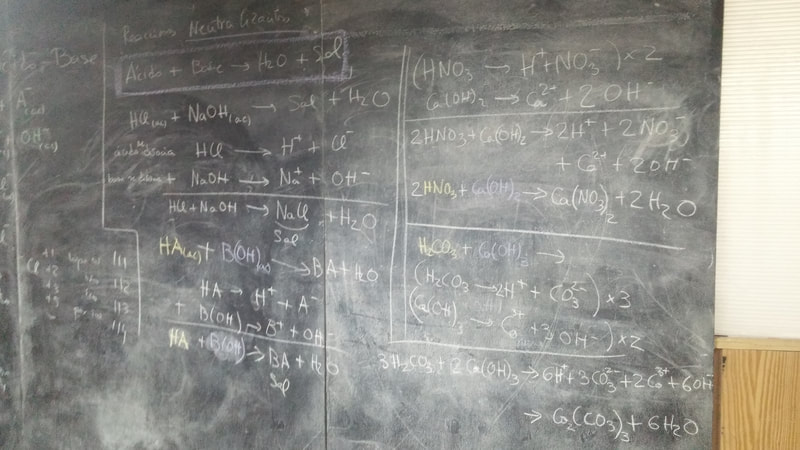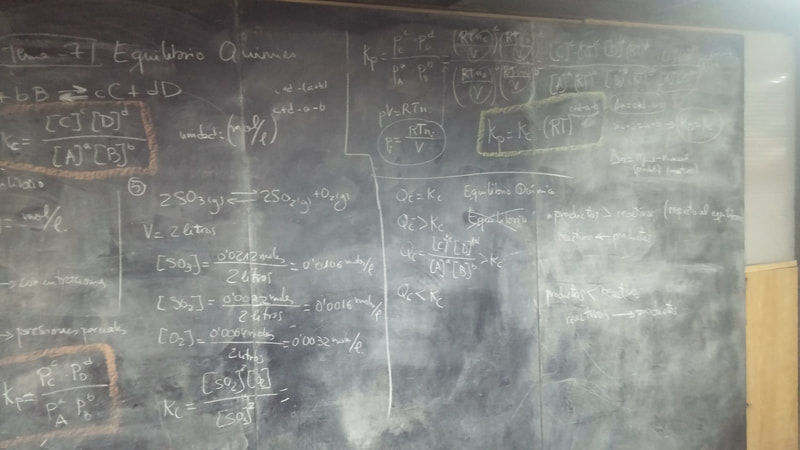Tareas para el próximo día 26 de NOVIEMBRE:
Ejercicios 1, 2, 3 y 1 de la pg. 64, tema - 3 del libro de Enlace Químico
_____________________________________________________________________________________________________________________________________________
EJERCICIOS para el próximo día 3 de Diciembre: 1, 2, 3 y 1 pg. 64; 4, 5 y 2 pg. 65
_____________________________________________________________________________________________________________________________________________
EJERCICIOS para el próximo día 10 de Diciembre: 3 pg. 66; 8,9 pg.67; 10, 4 pg.68; 11 pg.71; 12, 13, 5 pg.72
(el día 17 de diciembre tendremos examen tanto de Química como de Biología en las dos primeras horas)
21 ENERO 2019
28 ENERO 2019
11 FEBRERO
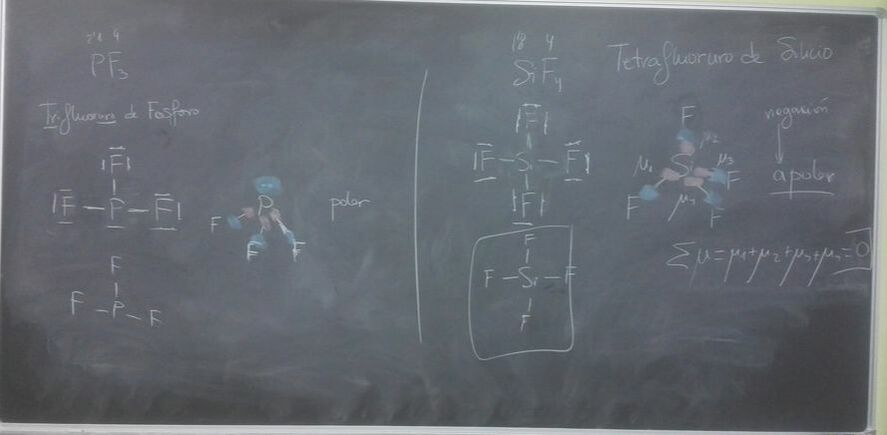
Llegamos hasta el final de los compuestos binarios. Corregimos ejercicios del libro
18 FEBRERO
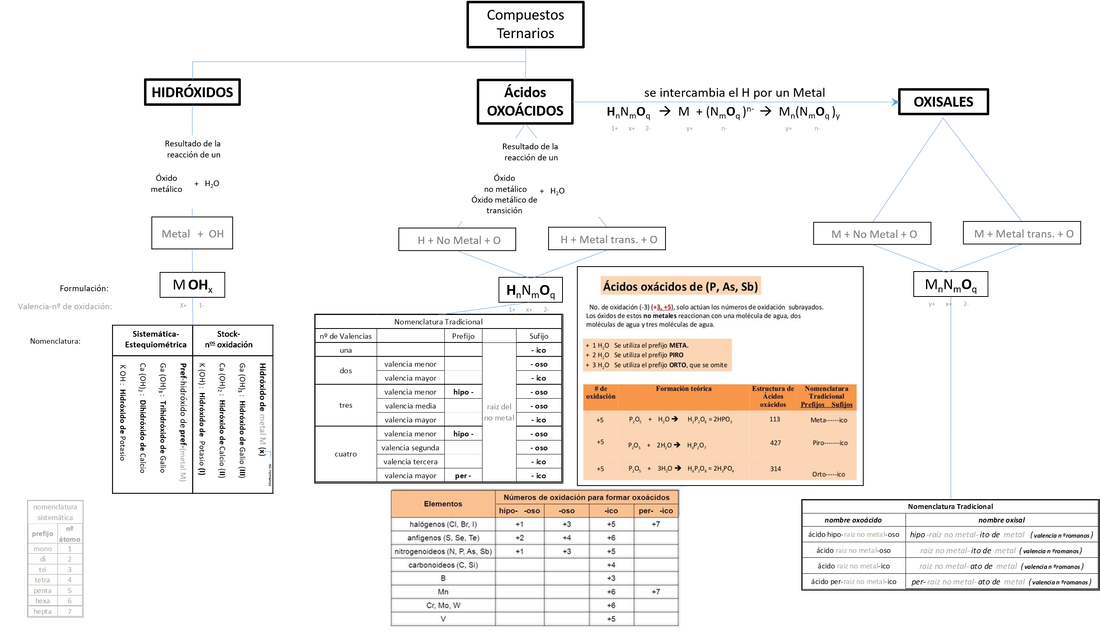
Vimos hasta los ácidos oxoácidos.
EJERCICIOS para el próximo día 25 de febrero: Ejercicio 8 pg. 97. Leer páginas 98 y 99, y hacer todos los ejercicios de las OXISALES hasta el 9 de la pg. 101.
www.acienciasgalilei.com/qui/formulacion/acidos%20oxoacidos.htm
25 FEBRERO
Vimos hasta la pg. 100.
EJERCICIOS para el 11 de marzo: 24 y 9 de la pg. 101
De la hoja que os di de masa molecular y concepto de mol, el ejercicio 8, y además NOMBRAR los compuestos cuyas masas molecular y molar debéis calcular en el ejercicio.
11 FEBRERO
Corregimos el ejercicio 8 que mandé el último día. Hicimos en clase el 11.
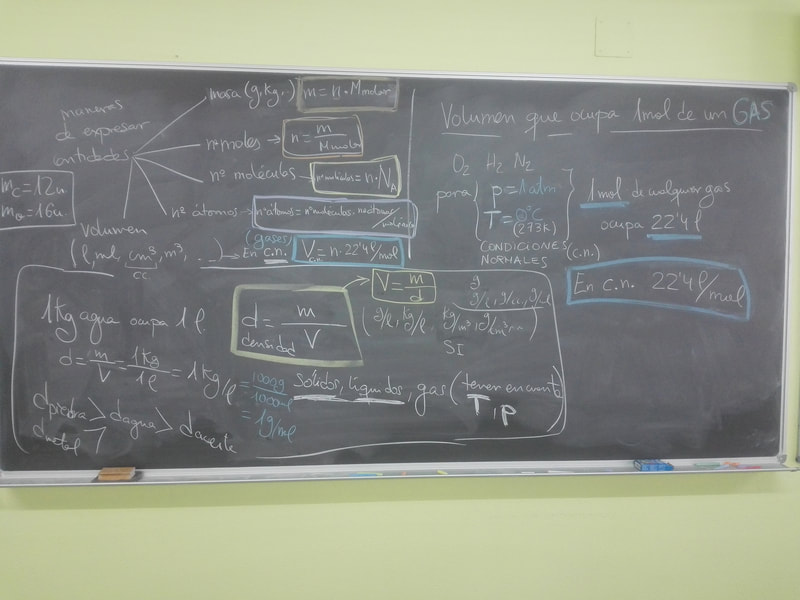
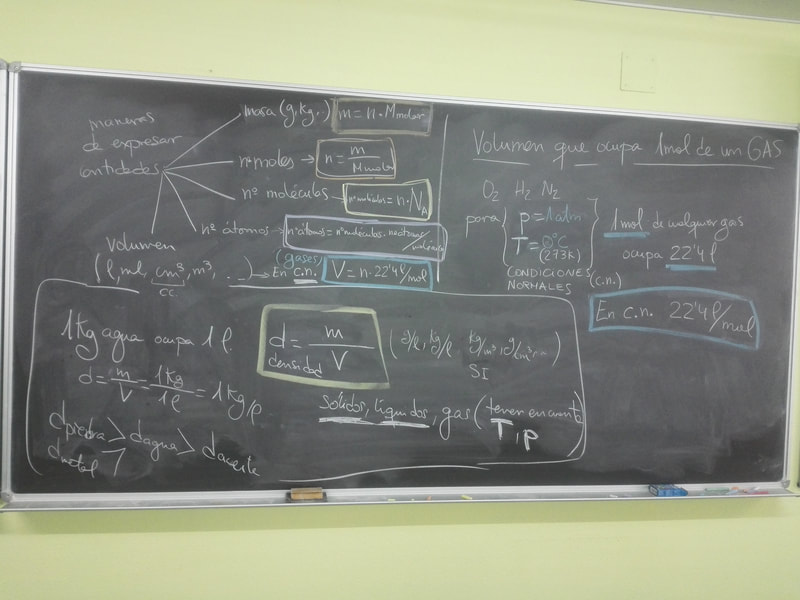
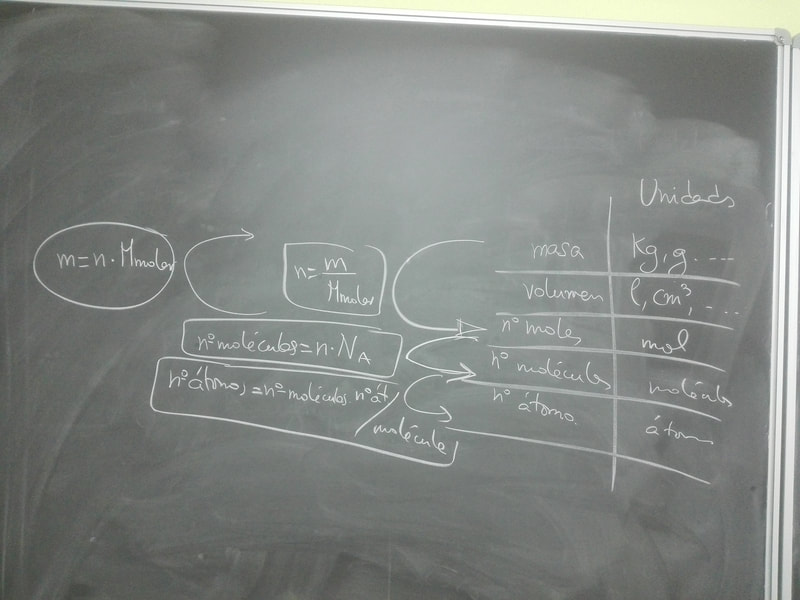
Terminamos de ver diferentes maneras de expresar cantidades, masa ( m ), nº de moles ( n ), nº moléculas, nº átomos, y volumen(V). Ejercicios 16 y 17 en clase.
Ya se pueden hacer todos los ejercicios de la hoja, aquí abajo os pongo el pdf.
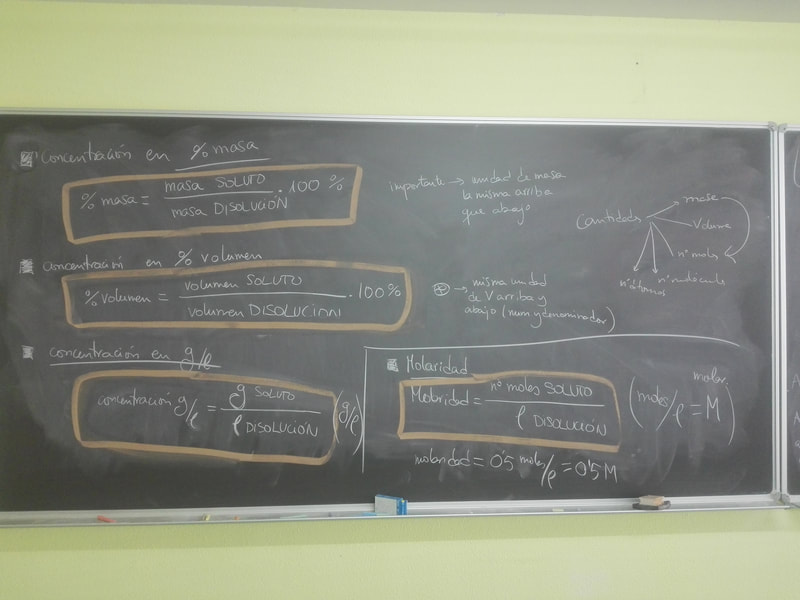
Próximo día, terminamos el tema 4. Veremos disoluciones, y diferentes maneras de expresar la concentración de una disolución.
18 MARZO
Vimos algunos ejercicios de la relación de problemas del concepto de mol, maza molecular, masa molar.
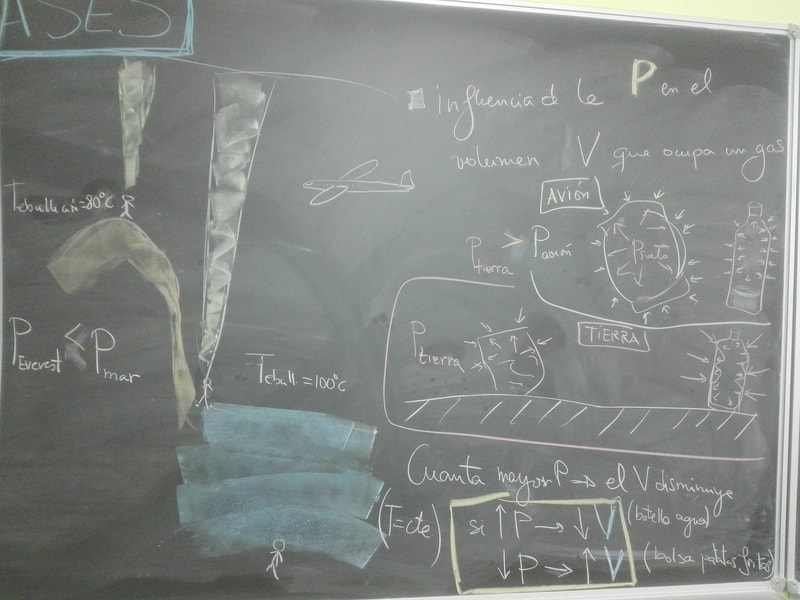
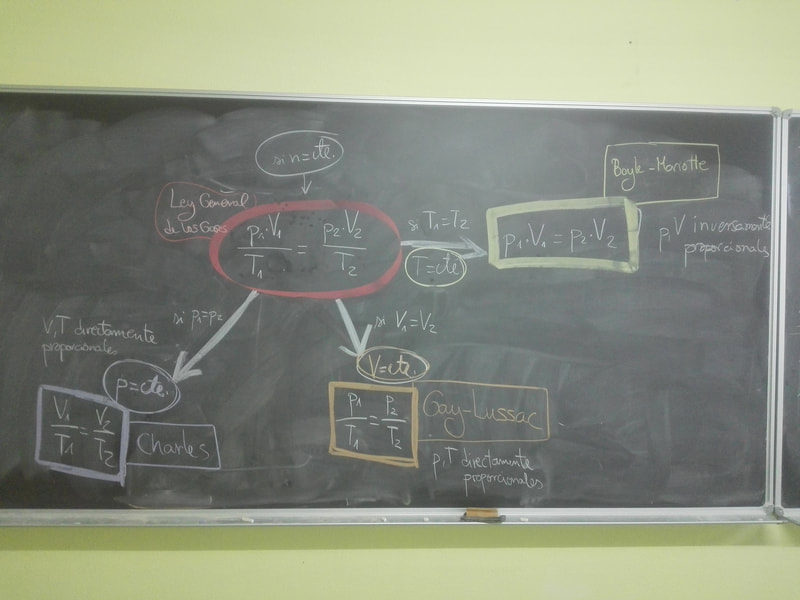
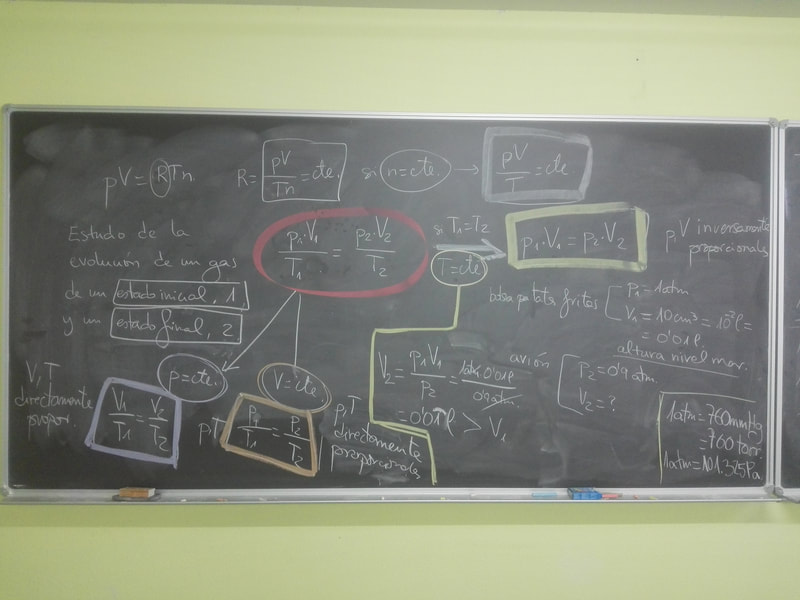
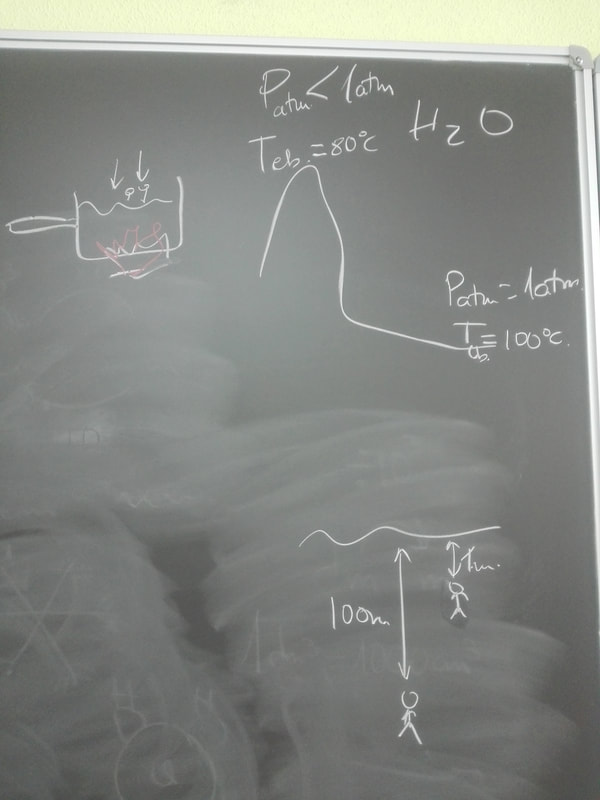
Di apuntes de GASES IDEALES, a partir de ella deducimos las tres leyes de los gases ideales. Próximo día resumen de las leyes de los gases.
EJERCICIOS para el próximo día 25 de marzo. Del 1 al 11 de los últimos apuntes que he dado.
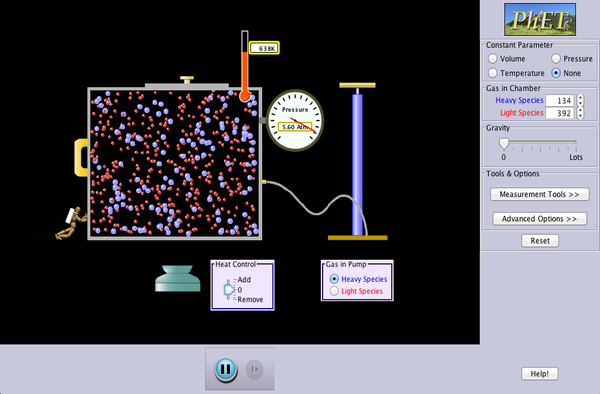
En el 3 y el 4 os puede servir de ayuda razonarlo con el applet adjunto más arriba.
25 MARZO
Terminamos Gases Ideales y comenzamos Disoluciones
Resultados ejercicios 10 y 11 de gases ideales:
10: (a) V = 33,58 L (b) V = 34,8 L (c) V = 16,17 L
11: (a) V = 56 L (b) V = 41 L (c) V = 35,9 L
EJERCICIOS para el 1 de abril, todos los de la hoja de disoluciones que quedan por hacer: del 14 al 21
Resultados:
14: concentración g/l = 100g/l ; molaridad = 1,79 M
15: concentración g/l = 500 g/l ; molaridad (que no lo pide el ejercicio por un error de escritura) = 6,8 M
16: concentración g/l = 200 g/l ; molaridad = 5 M
17: concentración g/l = 393 g/l ; % volumen = 9,32 % ; %masa = 30,23 %
18: concentración g/l = 456,8 g/l ; % volumen = 15,67 % ; % masa = 35,14 %
19: (a) m_soluto = 158 g ; m_disolvente = 800 g ; m_disolución = 958 g
(b) Ver imagen adjunta
(c) concentración g/l = 158 g/l
(d) %masa = 16,5%
(e) %volumen = 20%
20: (a) m_soluto = 250 g ; m_disolvente = 750 g ; m_disolución = 1000 g
(b) Ver imagen adjunta
(c) concentración g/l = 235,8 g/l
(d) %masa = 25%
(e) %volumen = 29,4%
(f) molaridad = 7,36 M
21: (a) m_soluto = 40 g ; m_disolvente = 750 g ; m_disolución = 790 g
(b) Ver imagen adjunta
(c) concentración g/l = 50 g/l
(d) %masa = 5,1%
(e) molaridad = 1,56 M
1 ABRIL
Corregimos un ejercicio de gases ideales, terminamos el tema de Disoluciones y pasamos a los temas 5 y 6 sin seguir exactamente el libro: REACCIONES QUÍMICAS, AJUSTES Y CÁLCULOS ESTEQUIOMÉTRICOS
EJERCICIOS para el próximo día 8 de abril:
De las fotocopias: 5, 6 , 7 y 1"ahora tú" de la pg. 117
Resultados 1"ahora tú" :
(a) H2 (g) + Cl2 (g) --> 2 HCl
Sínteis
(b) 2 KClO3 (s) --> 2 KCl (s) + 3 O2
Descomposición
(c) 3 H2SO4 (ac) + 2 Fe (s) --> 3 H2 (g) + Fe2(SO4)3 (ac)
Sustitución simple
(d) 3 HClO3 (ac) + Co(OH)3 (ac) --> Co(ClO3)3 (ac) + 3 H2O(l)
Sustitución doble
(e) C6H12 (g) + 9 O2 (g) --> 6 CO2 (g) + 6 H2O (g)
Sustitución doble
(f) CH4 (g) + 2 O2 (g) --> CO2 (g) --> CO2 (g) + 2 H2O (g)
Sustitución doble
- EJERCICIOS DE exámenes: 2º y 3º 2009 ; 2º y 4º 2010 ; 3º(a) y 4º 2011 ; 4º 2012 ; 3º 2013 ; 3º (a) y (c) y 4º 2014 ; 2º y 4º 2015 ; 4º (a) y (d) 2017
- Resultados:
4º 2006 : Lo veremos más adelante, cuando veamos las entalfías de reacción (la E que se absorbe o se libera en una reacción química)
2009 2º 2009 = 3º 2013 : (a) 0'125 moles (b) 0'45 moles/L= 0'45 M
3º : (a) 2 KClO3 --> 2 KCl + 3 O2 (b) V = 31'77 L (c) V = 28'6 L o m = 56'16 g
- 2010 2º: (a) N2 (g) + 3 H2 (g)--> 2 NH3 (g) (b) 0'3 moles
- 4º: (a) 0'25 moles (b) 15'63 cm3 = 0,016 L
- 2011 3º (a) 1 M
- 4º (a) n_HCl = 9 moles n_AlCl3 = 3 moles (b) n_Al = 0'3 moles n_HCl = 1 mol n_AlCl3 = 0'3 moles
- 2012 4º (a) H2S + Ca(OH)2 --> CaS + 2 H2O (b) 7'4 g (c) 0'5 L
- 2013 3º = 2º 2009
2014 3º : (a) 0'38 moles (c) NaOh + HCl --> NaCl + H2O Reacción de Sustitución Doble
- 4º : (a) 2 KClO3 --> 2 KCl + 3 O2 (b) 91'3 L
2015 2º : 2'56 g
4º : (a) 2 Na + 2 H2O --> 2 NaOH + H2
(b) Calculamos los moles de cada reactivo, de Na y de H2O. n_Na = 0'43 moles n_H2O= 0'56 moles.
El ajuste de la ecuación nos dice que por cada 2 moles de Na reaccionan 2 moles de H2O, es decir, cada mol de Na reacciona con 1 mol de H2O. Al tener 0'43 moles de Na y 0'56 moles de H2O, el reactivo que va a limitar va a ser el que está en menor cantidad (en nº de moles), que en este caso es el Na, el sodio.
- (c) 4'87 L (d) 2'3 g
2017 4º (a) 2 HCl + Mg(OH)2 --> MgCl2 + 2 H2O Sustitución Doble (d) 19 g
Todos los de la hoja adjunta: (Resolución en archivos posteriores)
- EJERCICIOS DE exámenes: 2º y 3º 2009 ; 2º y 4º 2010 ; 3º(a) y 4º 2011 ; 4º 2012 ; 3º 2013 ; 3º (a) y (c) y 4º 2014 ; 2º y 4º 2015 ; 4º (a) y (d) 2017
4º 2006 : Lo veremos más adelante, cuando veamos las entalfías de reacción (la E que se absorbe o se libera en una reacción química)
2009 2º 2009 = 3º 2013 : (a) 0'125 moles (b) 0'45 moles/L= 0'45 M
3º : (a) 2 KClO3 --> 2 KCl + 3 O2 (b) V = 31'77 L (c) V = 28'6 L o m = 56'16 g
2014 3º : (a) 0'38 moles (c) NaOh + HCl --> NaCl + H2O Reacción de Sustitución Doble
2015 2º : 2'56 g
4º : (a) 2 Na + 2 H2O --> 2 NaOH + H2
(b) Calculamos los moles de cada reactivo, de Na y de H2O. n_Na = 0'43 moles n_H2O= 0'56 moles.
El ajuste de la ecuación nos dice que por cada 2 moles de Na reaccionan 2 moles de H2O, es decir, cada mol de Na reacciona con 1 mol de H2O. Al tener 0'43 moles de Na y 0'56 moles de H2O, el reactivo que va a limitar va a ser el que está en menor cantidad (en nº de moles), que en este caso es el Na, el sodio.
2017 4º (a) 2 HCl + Mg(OH)2 --> MgCl2 + 2 H2O Sustitución Doble (d) 19 g
Todos los de la hoja adjunta: (Resolución en archivos posteriores)
Vídeo que muestra la reacción química de descomposición del óxido de mercurio : 2HgO(s) --> 2Hg(l) + O2(g)
8 ABRIL
Corregimos ejercicios principalmente de ajuste de ecuaciones químicas e identificación del tipo de ecuación
Vimos qué era la entalpía, ΔH , y qué valores de ΔH indican que la reacción sea endotérmica (ΔH> 0) u exotérmica (ΔH<0).
EJERCICIOS para vacaciones:
Hacer todos los que mandé la semana anterior
Ejercicios "AhoraTú" 2, 3, 4 y 5 del Tema 5 (mirad/haced los ejercicios resueltos)
"AhoraTú" 1, 2, 3, 4, 5 y 6 del Tema 6 (son similares a los de la hoja de ejercicios que os dí, mirad/haced los ejercicios resueltos)
Resultados ejercicios "AhoraTú" 2, 3, 4 y 5 del Tema 5:
Resultados "AhoraTú" 1, 2, 3, 4, 5 y 6 del Tema 6:
1º (a) 3'06 moles (b) 152'04 moles
2º (a) 434'9 g (b) 23'73 l
3º Si se necesitan más gramos de B que de A para que ambos reactivos reaccionen al completo, en proporción 16 a 12, y tenemos que partir de la misma cantidad de A y B, 6 g., el reactivo que limitará la reacción (reactivo limitante), va a ser el B. Por tanto, tomaremos como referencia los gramos de B, 6g.
m_C= 3'75 g. m_D= 6'75 g.
4º (a) Como para que ambos reactivos reaccionen por completo, se necesita el mismo número de moles, al poseer de partida, más moles de H2O que de Na, el reactivo que va a limitar va a ser el que tiene menor cantidad, es decir, el Na. Así que tomaremos como referencia la cantidad de moles de sodio, Na.
Reactivo limitante: el sodio, Na
(b) 17'2 g de NaOH.
5º 3'27gramos de Zn 0'05 moles de Zn(NO3)2
6º (a) 32'9 g de FCl (b) 8'02 l de H2
EJERCICIOS de exámenes : 4º 2009 ; 1º 2013
24 ABRIL
Ejercicios Finales del tema 5 resueltos
Ejercicios de Exámenes:
- 2º 2006 R. Ácido - Base
- 3º 2006. Equilibrio y Ácido - Base ( grado de disociación en pg. 192 )
- 5º 2006 Equilibrio Químico
- 2º 2007 R. Ácido - Base
- 5º 2007 Equilibrio y Ácido-Base ( grado de disociación en pg. 192 )
- 3º (b) 2011 Ácido- Base
- 3º 2012 Ácido - Base
- 3º (b) 2014 Ácido - Base
- 4º (b) (c) 2017 Ácido - Base
27 ABRIL
EJERCICIOS "Ahora Tú" - tema 7 - Equilibrio Químico
EJERCICIOS Cuestionario Final - tema 7 - Equilibrio Químico
EJERCICIOS "Ahora Tú" - tema 8 - Reacciones ÁCIDO - BASE
EJERCICIOS - Cuestionario Final - tema 8 - Reacciones ÁCIDO - BASE
6 MAYO
Ejercicio de EXAMEN de reacciones REDOX:
| ejercicios_resueltos_ajuste_ecuaciÓn_quÍmica_mÉtodo_iÓn-electrÓn.pdf | |
| File Size: | 1111 kb |
| File Type: | |